
(オープニングタイトル)

レモンを2つに切って、銅と亜鉛の金属の板を差し込みます。これを導線で電圧計につなぐと、なんと、針が動きました。レモンと金属の板が、電池のはたらきをする。どういうことでしょう。

いろいろな水溶液で、電流が流れるか調べてみましょう。まずは蒸留水。電源と豆電球をつないだ電極を入れると…。電流は流れません。食塩水はどうでしょう。豆電球がつきました。電流が流れています。食塩のように、水に溶けて電流が流れる物質を「電解質(でんかいしつ)」といいます。砂糖水ではどうでしょう。電流は流れません。砂糖のように、水に溶けても電流が流れない物質を「非電解質」といいます。物質には、水に溶かしたとき、電流が流れるものと電流が流れないものがあるのです。

電解質である塩化銅の水溶液に電極をさして、電流を流してみましょう。電源につないだ陽極からは、気体が発生しています。陽極近くの水溶液をとってにおいをかいでみると、特有の刺激臭があります。塩素です。一方、陰極には、赤茶色の物質がついています。銅です。塩化銅が、塩素と銅に分解されたのです。これはどういうことでしょう。
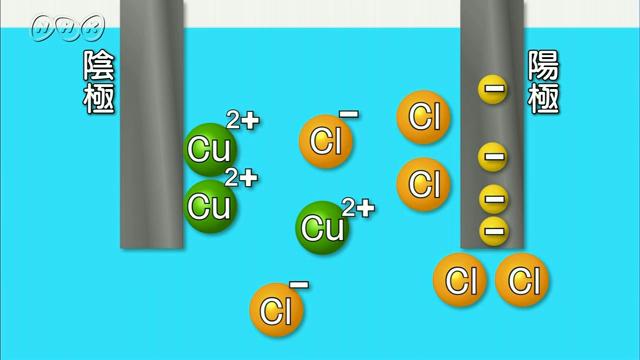
塩化銅は、水に溶けると電子が移動して、プラスの電気を持った銅イオンとマイナスの電気を持った塩化物イオンに分かれます。電流が流れるとき、陽極にはマイナスの電気を持った塩化物イオンが集まり、陰極にはプラスの電気を持った銅イオンが集まります。そして塩化物イオンは陽極に電子を渡して塩素原子になります。その塩素原子2個がすぐに塩素分子になり、気体として発生したのです。一方、陰極では銅イオンが電子を2個もらって銅原子になり、陰極に付着したのです。このように、電解質の水溶液に電流を流すと、イオンが水中を移動して電流が流れ、化学変化も起きるのです。

電池は私たちの生活に欠かせないものになっています。電池はどのようにして電気を得ているのでしょうか。実際に電池を作ってみましょう。備長炭という木炭に、食塩水を染み込ませたペーパータオルを巻き、その上からアルミニウム箔(はく)を巻き付けます。これで電池の完成。木炭とアルミニウム箔の部分にクリップをはりつけ、モーターにつなぐと、モーターが動き出しました。電流が流れているのです。何が起こっているのでしょう。
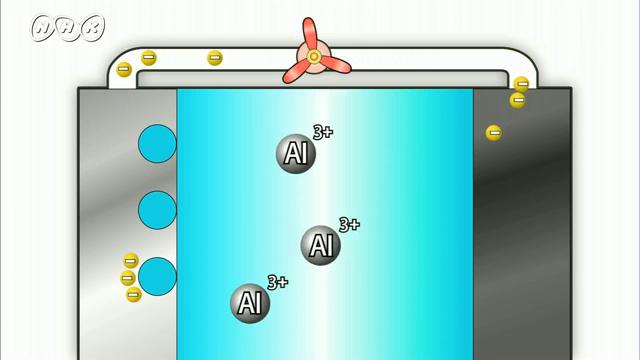
アルミニウムは、食塩水に溶けてアルミニウムイオンになります。アルミニウム箔(はく)には電子が残ります。この電子が導線を通って備長炭に移動すると、電流が流れ、プロペラが回転するのです。電流を長時間流したあと、アルミニウム箔はイオンになって溶け出したため、ボロボロになっています。このように、電池は金属がイオンになって溶け出る性質を利用して、電気エネルギーを作り出しているのです。

金属は、種類によってイオンになりやすさが違います。これを「イオン化傾向」といいます。マンガン、アルミニウム、亜鉛などはイオン化傾向が大きく、水銀、銀、金などはイオン化傾向の小さい金属です。電池では、2つの金属を電解質の水溶液に入れたとき、イオン化傾向の大きいほうの金属が陰極(-極、負極)となり、小さいほうの金属が陽極(+極、正極)となります。2種類の金属のイオン化傾向の差が大きいほど、電圧は大きくなります。(※電位の高い方を陽極とした場合)

これを利用して最初に電池を作ったのは、イタリアの物理学者ボルタです。ボルタは、亜鉛と銅、うすい硫酸を使い、電池を作りました。ボルタの電池の導線をモーターにつなぐと、はじめは勢いよく回りますが、すぐに電圧が下がり、動きが悪くなります。また、持ち運ぼうとするとき液がこぼれるなど、実用的ではありませんでした。

それを改良したのが、マンガン乾電池です。電極には亜鉛と二酸化マンガンを使い、電解液の塩化亜鉛水溶液を、二酸化マンガンと炭素の粉末で練り合わせて液がこぼれないようにしました。この乾電池を発明したのは日本の屋井先蔵(やい・さきぞう)です。その後開発されたのが、アルカリ乾電池。電解液にアルカリ性の水酸化カリウム水溶液を使い、マンガン乾電池よりも大きな電流が長く得られるようになりました。
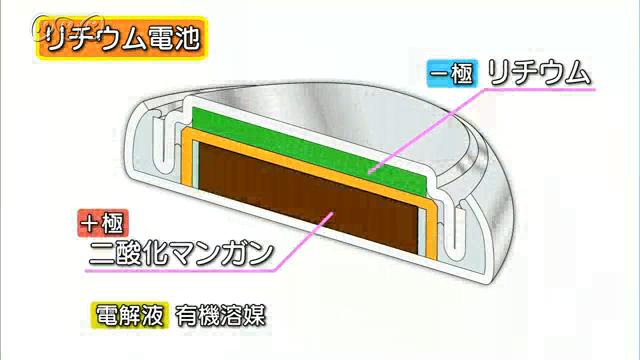
腕時計などに使われているリチウム電池は、イオン化傾向がより大きいリチウムを電極に使い、高い電圧を得ることができます。さらに、日本で実用化されたリチウムイオン電池は、コバルト酸リチウムを電極に使い、小さくても、高い電圧、大きな電流が得られます。このように、より長持ちで、よりパワーのある電池を開発するため、日々研究が続けられているのです。